Sauerstoff ist ein für die Funktion unseres Körpers dringend benötigter Bestandteil. Sauerstoff liegt in unserem Körper in einer an das Hämoglobin gebundenen Form (SpO2 Normwert 95-100 %) sowie einer im Plasma gelösten Form (PaO2 Normwert 70 – 105) vor. Hierbei sind ca. 97 % gebunden und 3 % im Plasma gelöst vorzufinden. Regelmäßig messen wir die Sauerstoffsättigung (SpO2) im Rettungsdienst. Können wir auf eine Blutgasanalyse zurückgreifen, z. B. im Intensivtransport, steht uns auch der arterielle Sauerstoffpartialdruck (PaO2) zur Verfügung. Beide stehen in einer gewissen Relation zueinander. Diese Relation kann man anhand einer grafisch dargestellten Kurve, der Sauerstoff-Hämoglobin Bindungskurve, darstellen. Der Name deshalb, weil sie eine Aussage über die Bindung von Sauerstoff zum Hämoglobin darstellt. Die Kurve verläuft nicht linear sondern fällt nach einem anfänglich relativ seichtem Verlauf steil ab. Die sigmoidal verlaufende Kurve zeigt also den Oxyhämoglobinwert bei in der x-Achse gezeigten pO2 Werten an. Je nach Verschiebung dieser Bindungskurve nach links oder rechts kommt es zu einer Verschiebung der Affinität von Sauerstoff zum Hämoglobin.
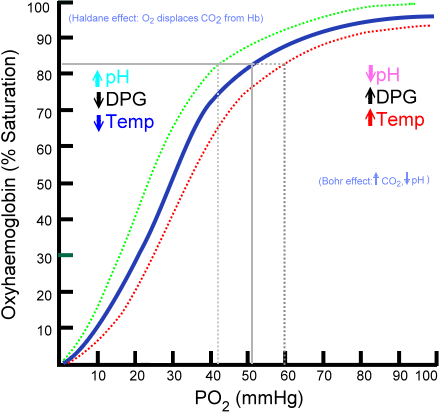
In der Theorie lassen sich die beiden Werte bei nicht allzu großer Verschiebung der Kurve also auch im Rahmen der 4-5-6-7-8-9 Regel [1] grob erahnen:
SpO2 70 = pO2 40
SpO2 80 = pO2 50
SpO2 90 = pO2 60
In Verbindung mit SpO2 und pO2 noch zwei wichtige Begriffe welche gerne verwechselt oder gleichgestellt verwendet werden:
Hypoxämie = pathologisch erniedrigter SpO2 Wert im Blut (Hämoglobin ist nicht richtig aufgesättigt)
Hypoxie = Sauerstoffmangel auf Zellebene mit fatalen Folgen im Zellstoffwechsel
Eine Grundkenntnis über die Verschiebungsmöglichkeiten dieser Kurve sowie die darauf Einfluss nehmenden Parameter ist deshalb nicht ganz unwichtig weil es damit wie oben bereits erwähnt auch zu einer Verschiebung der Affinität des Sauerstoffes an das Hämoglobin kommt; also wie gut haftet der Sauerstoff am Hämoglobin. Dies wiederum wirkt auf die Sauerstoffaufnahme in der Lunge aber auch auf die Sauerstoffabgabe an die Zelle ein.
Ein globaler Shift, also eine Verschiebung der Bindungskurve im gesamten Körper, wäre „the worst case“. Ein Shift kann jedoch auch örtlich, auf Systeme begrenzt auftreten. Dies ist in verschiedenen Bereichen sogar physiologisch gewollt um z. B. die Sauerstoffabgabe z. B. zu fördern. Hierzu auch eine gute Erörterung im folgenden YouTube Video (…leider auf Englisch)
Eine Linksverschiebung führt zu einer erhöhten Affinität des Sauerstoffes an das Hämoglobin. Dies bedeutet er wird in der Lunge leichter an das Hämoglobin gebunden, jedoch auf Zellebene schlechter an diese abgegeben.
Bei einer Rechtsverschiebung kommt es zu einer Herabsetzung der Affinität des Sauerstoffes zum Hämoglobin. Sauerstoff wird also in der Lunge schlechter an das Hämoglobin gebunden aber leichter an der Zelle wieder abgegeben.
Die am meisten für eine Verschiebung verantwortlichen Faktoren sind
- pH Wert (H+ Ionen)
- 2.3 DPG (Beiprodukt der Glykolyse)
- Temperatur
Für eine Linksverschiebung sorgt jeweils eine niedrige Temperatur, ein erniedrigter 2.3 DPG Wert sowie eine niedrige Anzahl von H+ Ionen, also ein hoher pH Wert.
Für eine Rechtsverschiebung demnach eine erhöhte Temperatur, ein erhöhter 2.3 DPG Wert sowie eine hohe Anzahl von H+ Ionen, ein niedriger pH Wert.
Verwirrend…? Ja, eigentlich schon – aber mit einer Eselsbrücke ganz gut einzuprägen…
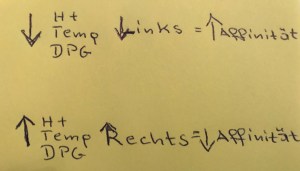
Zwei Beispiele….
Verabreichung mehrerer, nicht wirklich erwärmter Ery-Konzentrate führt zu einer Herabsetzung der Körpertemperatur sowie zu einem erniedrigten 2.3 DPG da dieses in den Konserven aus den Erythrozyten entweicht. Folge ist eine Linksverschiebung der Sauerstoff-Hämoglobin Bindungskurve. Der Sauerstoff wird bei diesem Patienten zwar gut aufgenommen und an das Hämoglobin gebunden; es reicht u. U. ein pO2 von 40 um eine SpO2 von knapp über 80 zu erreichen. Jedoch erschwert sich die Sauerstoffabgabe an die Zelle.
Ein Patient mit einer Azidose, also einem hohen H+ Ionen Wert (niedriger pH) und Fieber muss eher mit einer Rechtsverschiebung rechnen. Der Sauerstoff wird schwerer an das Hämoglobin zu binden und für eine SpO2 von ebenfalls knapp über 80 bereits ein pO2 von ca. 60 notwendig sein. Die Abgabe des für die Zelle lebensnotwendigen Sauerstoffes erfolgt hier jedoch sehr gut.
Nicht zuletzt versinnbildlicht die Sauerstoff-Hämoglobin Bindungskurve aber auch sehr deutlich warum die Sicherheitszone der SpO2 bei einer Intubationsnarkose nicht erst bei 90 % SpO2 sondern viel eher enden sollte. Vergleicht man diese Kurve mit einer Wasserrutsche so wird man feststellen dass spätestens bei 90 % SpO2 der Absturz ins kalte Wasser, sprich Sättigungsabfall ins Unendliche, sehr rapide von statten gehen wird. Und dieses Verständnis ist elementar wichtig.


2 Gedanken zu „Die Sauerstoff-Hämoglobin Bindungskurve“